KMnO4=K2KMnO4 MnO2
来源:学生作业帮助网 编辑:作业帮 时间:2024/05/04 06:38:55
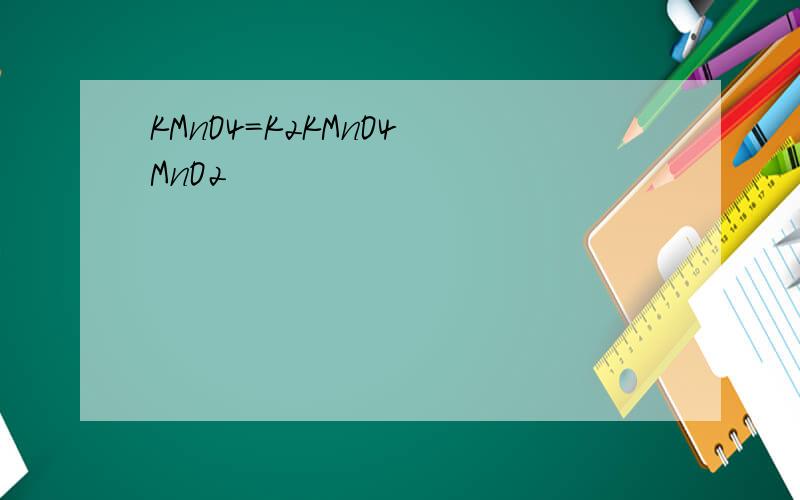
两个反应都是分解反应,分解反应全都是氧化还原反应高锰酸钾和氧化汞在反应中既是氧化剂也是还原剂理由是化学书上的话:化合价升高,失电子被氧化,是还原剂.化合价降低,得电子,被还原,氧化剂.
KMnO4既是氧化剂又是还原剂原因:KMnO4中的Mn为正7价,K2MnO4中的Mn为正4价,化合价降低,得电子,被还原.KMnO4中氧元素为负2价,O2中氧元素为0价,化合价升高,失电子,被氧化.所
2分子高锰酸钾受热分解为一分子的锰酸钾,一分子的二氧化锰还有一分子的氧气
这个问题很好回答,可是很不容易让你明白2KMnO4=K2MnO4+MnO2+O2这个化学方程式表示2分子KMnO4,分解为1分子K2MnO4+1分子MnO2+1分子O2为什么等号右面不写成:K2Mn+
K2MnO4中K有两个,根据化学方程式等号两边守恒原则,KMnO4前面必须也得有2,.
2KMnO4=K2MnO4+O2↑+MnO2
3H2SO4+2KMnO4+5K2SO3=6K2SO4+2MnSO4+3H2O
解题思路:反应物中无硫酸根离子,产物中的硫酸根离子均来自二氧化硫,即二氧化硫全部被氧化成了硫酸根离子,故应该全部计算。解题过程:解答:2KMnO4+5SO2+2H2O==2MnSO4+K2SO4+2H
为什么这么多问配平的啊?这么难啊?哥从来都是看下化合价就出来了~占楼,这会在看韩国SC直播2KMN04+5H2S+3H2SO4=K2SO4+2MNSO4+5S+8H2O
5C+4KMnO4+6H2SO4==5CO2+4MnSO4+2K2SO4+6H2O
有机化学的学习中,经常用到高锰酸钾溶液.做试剂用时有酸性、中性及碱性高锰酸钾溶液三种.其中酸性高锰酸钾溶液氧化性最强,应用也最广.乙烯遇到中性及碱性高锰酸钾溶液,当试剂不足量时,乙烯的氧化产物是乙二醇
正确答案是:5SO2+2MnO4-+2H2O==2Mn2++5SO42-+4H+这是很少见的与高锰酸钾反应生成氢离子的.其他和高锰酸钾反应的比如草酸、氯离子、亚铁离子等都是消耗氢离子.希望对你有所帮助
2KMnO4+3H2C2O4+5H2SO4==K2SO4+2MnSO4+10CO2+8H20
2KMnO4+16HCl=2MnCl2+5Cl2+2KCl+8H2O5:1;转移10电子
把K2MnO4=KMnO4+MnO2+O2改成2KMnO4=K2MnO4+MnO2+O2
二KMnO4+五Na2SO3+三H2SO4==K2SO4+五Na2SO4+二MnSO4+三H2O二KMnO4+Na2SO3+二NaOH==二Na2MnO4+K2SO4+H2O二KMnO4+三Na2SO
首先:1、双氧水中的O显-1价,氧化性和还原性都有,具体表现什么性质要看具体反映,决定于与它反映的物质氧化性和还原性的相对强弱,另外还有非常微弱的酸性.2、高锰酸钾中的Mn显+7价,可以降低到+6,+
2KMnO4+3Na2SO3+H2O==2MnO2+3Na2SO4+2KOH
这个是高锰酸钾制氧气的,应为2KMnO4==K2MnO4+MnO2+O2,即在左边加2,右边不变反应条件是加热,O2右边要打向上的箭头.
用双线桥的话要用三条线,氧一条,高锰的锰分出两条,分别到锰酸钾和氧化锰.这个化学式双线桥不好连,我记得课本上是把它作为化合价升降法的例子出现的.